首先观察神经元和肿瘤之间的相互作用,可以揭示形成、扩散
哈佛医学院神经肿瘤学家 Annie Hsieh 每周都会治疗神经胶质瘤患者,神经胶质瘤是最常见的脑癌类型,包括最致命的胶质母细胞瘤。
她说,在 Hsieh 的神经外科医生同事通过手术切除神经胶质瘤后,通常看起来没有留下任何癌症。随后可能会进行放疗和其他治疗。然而,神经胶质瘤往往会复发,不仅在原始部位,而且在大脑的远处部位,威胁到神经损伤,在某些情况下甚至死亡。
大脑中发生了什么事情来促使这些肿瘤在那里再生,而很少出现在身体的其他部位?几十年来,这个问题一直困扰着科学家,并使神经胶质瘤成为最难治疗的癌症之一。这也是 Hsieh 医生科学家长期以来一直想解开的一个谜团。
现在,她和 HMS 合作者首次展示了大脑中与神经胶质瘤相连的神经元类型,从而填补了一块拼图。
该团队的调查结果周三在 PNAS 上报告。
分析小鼠中这种神经胶质瘤支配神经元的身份和特性,为驱动这些癌症在大脑中形成和扩散的因素提供了新的见解。这些发现还可以帮助研究人员设计新的治疗策略来阻止这些肿瘤复发。
“这是第一步,它为为什么肿瘤可以在大脑中无处不在提供视觉解释,”该研究的第一作者、麻省总医院神经病学 HMS 讲师 Hsieh 说。“我们现在可以看到连接的神经元起源,研究它们如何与神经胶质瘤整合,并寻找中断生长的机会。”
“神经网络如何运作以及这些超级可怕的肿瘤如何整合并渗透到整个神经系统中,这令人着迷。”
Annie Hsieh,神经肿瘤学家
该研究克服了可视化和分析与神经胶质瘤相关的神经元的长期障碍,并展示了一种更广泛地推进肿瘤与神经系统之间相互作用研究的方法。
Hsieh 在 Bernardo Sabatini 实验室担任神经生物学研究员,并在 HMS 布拉瓦尼克研究所的 Marcia Haigis 实验室担任细胞生物学研究员时进行了这项工作。Haigis 和 Sabatini 是该研究的共同高级作者。
神经胶质瘤如何破坏网络
神经胶质瘤起源于神经胶质细胞,神经胶质细胞在塑造和维持神经回路方面发挥重要功能。科学家们已经知道神经元会在神经胶质瘤细胞上形成突触,但他们看不到这些神经元的另一端(细胞体)在大脑中的位置。这掩盖了神经元的身份。
Hsieh 和团队成功地使用狂犬病病毒将神经胶质瘤支配神经元追溯到它们的来源,狂犬病病毒被设计为仅感染特定的感兴趣细胞,并在进入时照亮这些细胞。病毒从肿瘤细胞通过连接到它的神经元传回去。
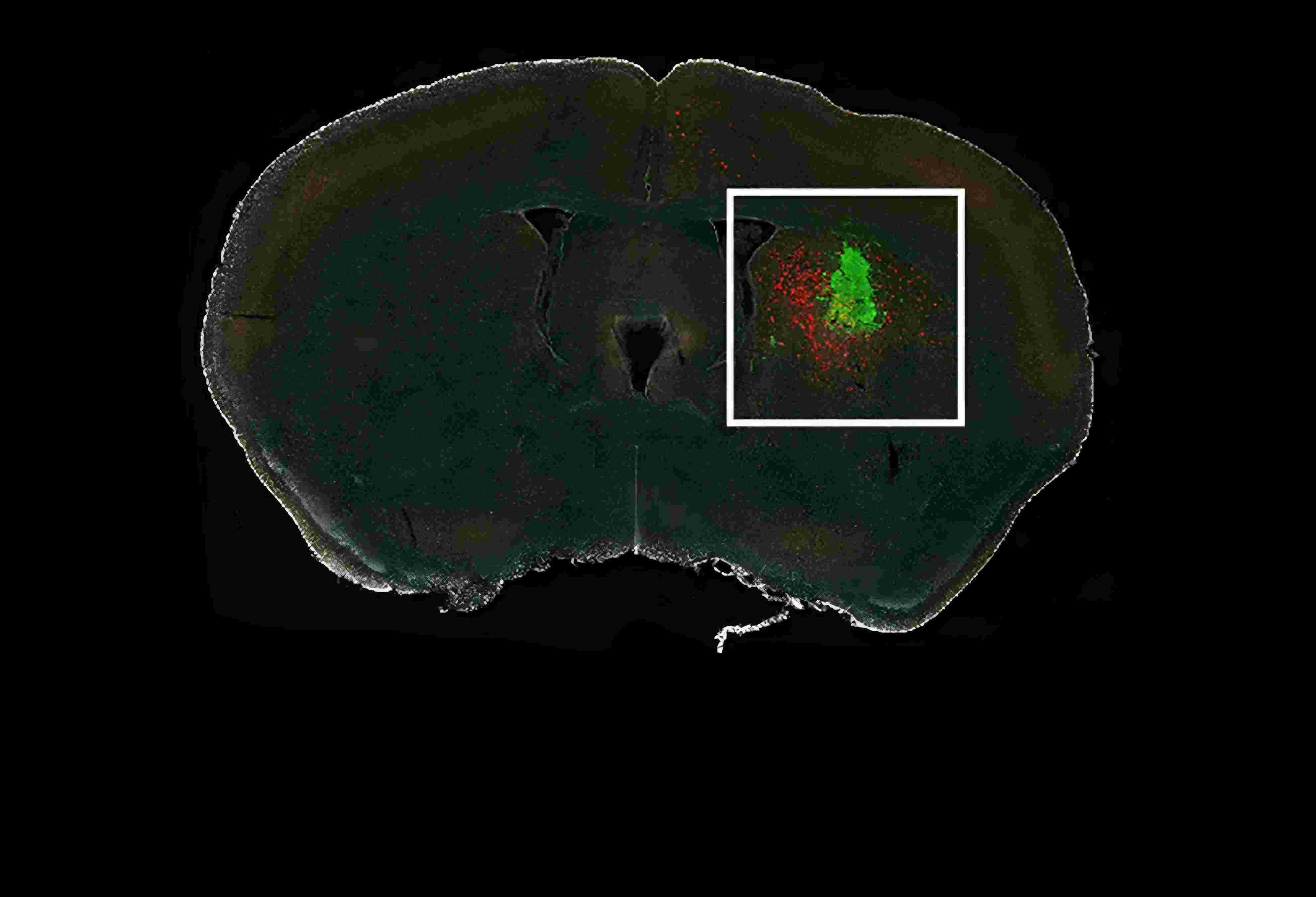
研究人员将人类神经胶质瘤细胞注射到小鼠的大脑中,并等待神经元与肿瘤连接。然后,他们应用狂犬病病毒来点亮感兴趣的细胞。很快,他们就有了一张照亮小鼠大脑的照片,显示了导致神经胶质瘤的所有发光神经元。
图谱显示,神经胶质瘤与现有的神经元布线模式挂钩。
“电线已经在那里了;神经胶质瘤只是连接到它们,“Hsieh 说。“他们劫持了已经存在的东西,而不是形成自己的任意连接。”
研究人员观察到,这些神经元起源于大脑的整个领域。
“它们从大脑内部一直来到肿瘤,”Hsieh 说。“神经网络如何运作以及这些超级可怕的肿瘤如何整合并渗透到整个神经系统中,这令人着迷。”
揭开神经元的秘密身份
研究小组发现,大多数从大脑远处延伸的神经胶质瘤神经胶质瘤神经元都是产生谷氨酸的类型,谷氨酸是激发神经元的主要大脑化学物质。这一发现与之前的观察结果一致,即神经元兴奋刺激神经胶质瘤生长,并且神经元-神经胶质瘤通讯涉及谷氨酸。
然而,影响深远的神经胶质瘤神经的子集显示出它们同时产生谷氨酸和另一种称为 GABA 的化学物质的迹象,这种化学物质会抑制神经元活动。在一些大脑区域,来自肿瘤部位附近的神经胶质瘤神经胶质瘤神经元似乎在很大程度上是 GABA 能的。
结果表明,与神经胶质瘤细胞相互作用的神经元比目前认识到的更加多样化。这对肿瘤生长和扩散的影响尚不清楚。
“我们看到肿瘤与任何地方都相连。这些联系是否为他们提供了通往任何地方的途径,这是我们需要研究的事情,“Hsieh 说。
该团队探测了神经胶质瘤支配神经元的电特性,发现它们与没有神经胶质瘤的大脑中的类似神经元之间存在某些差异。正常神经元和神经胶质瘤神经之间或神经元-神经元和神经元-神经胶质瘤相互作用之间的这种变化为像 Hsieh 这样的研究人员提供了宝贵的线索,他们寻求在保持正常功能的同时干预癌症过程的方法。
Hsieh 说,开发神经胶质瘤治疗方法的需求是紧迫的。她指出,研究人员曾尝试用对其他类型癌症有效的药物治疗神经胶质瘤,但大多数都失败了。
“通过解开神经胶质瘤-神经元相互作用的驱动因素并确定独特的机制,我们可以探索中断它们的策略,有可能阻止肿瘤的轨迹并防止它们复发,”Hsieh 说。
尽管她知道实验室中的发现还需要很多年才能转化为她的神经胶质瘤患者和世界各地其他人的治疗方法,但 Hsieh 仍然乐观地认为这些最新的见解可以帮助推动该领域向前发展。
“它还没有离诊所很近,”她说,“但它向前走了一英寸。
其他作者包括 Sanika Ganesh、Tomasz Kula、Madiha Irshad、Emily A. Ferenczi、Wengang Wang、Yi-Ching Chen、Song-华 胡、Zongyu Li 和 Shakchhi Joshi。
这项工作得到了美国国立卫生研究院(包括美国国家癌症研究所奖 K12CA090354)、霍华德休斯 r 研究所、鲁宾家庭基金会学者奖、美国神经病学学会、巴勒斯惠康基金、HMS 路德维希中心和格伦医学研究基金会的支持。共聚焦图像是在HMS的成像技术和教育核心获取的,荧光原位杂交是由HMS的神经生物学成像设施进行的。
Haigis 获得了 Agilent Technologies 和 ReFuel Bio 的研究资助;在 Alixia、Minovia Therapeutics 和 MitoQ 的科学顾问委员会任职;是 Cell Metabolism 和 Molecular Cell 的编委;并且是 ReFuel Bio 的顾问和创始人。
来源:https://news.harvard.edu


